BÉRCES TIBOR
A fizikokémius Polányi Mihály
Polányi Mihály neve jól ismert a fizikai-kémia1-3 és a filozófia3-5 mûvelõinek körében, de munkásságának jelentõsége korántsem ismert szélesebb körökben olyan mértékben, mint amit ez a nagy formátumú, kreatív egyéniség megérdemelne. Polányi Mihály színes egyéniségét és rendkívül sokrétû tevékenységét bizonyítja az a tény, hogy jelentõs eredményeket ért el a kémiában, a fizikában, a közgazdaságtanban és a filozófiában is. Ebben az elõadásban csak a fizikokémikus Polányi Mihályról fogok beszélni. Ez sem könnyû feladat, hiszen ilyen irányú munkássága a fizikai kémiának legalább négy jól körülhatárolható területére terjedt ki, nevezetesen az adszorpció, az anyagok rugalmassági és szilárdsági viszonyai, a röntgendiffrakciós analízis és végül, de nem utolsó sorban a reakciókinetika és reakciómechanizmusok kutatása területére.
Sokakban, sokunkban felmerült a kérdés, hogy mi a titka ennek a sokoldalúságnak és páratlan kreativitásnak. A válasz erre a kérdésre nyilvánvalóan csak összetett lehet. Az azonban bizonyos, hogy rendkívül eredményes tudományos munkásságában döntõ szerepet játszott vele született rendkívüli tehetsége és a szülõi házban szerzett ismeretei, benyomásai.
Polányi Mihály 1891. március 12-én született Budapesten a felvidéki zsidó vasútépítési vállalkozó, Pollacsek Adolf és a litván származású Wohl Cecilia utolsó gyermekeként. (A családi nevet 1904-ben változtatták meg Polányira.) Testvérei közül a legidõsebb, Laura történész és könyvtáros szakember, Károly pedig világhírû közgazdász volt. A következõ generáció tagjai között is több hírességet találni, elég ha Mihály fiára, a Nobel-díjas kémikus John C. Polanyira hivatkozom.
A család meghatározó egyénisége az édesanya volt, akit mindenki Cecil mamaként ismert. Nagymûveltségû asszony volt, a századforduló utáni pesti társaság egyik központi alakja, akinek a szalonjában számos kiválóság, az akkori idõk legismertebb mûvészei, írói, tudósai gyakran megfordultak. Ez a társasági élet kétségtelenül befolyásolta a Polányi család gyermekeinek, köztük Mihálynak a fejlõdését, egyéniségük kibontakozását. Mindezt hasznosan egészítette ki az az igényes neveltetés, amit az apa gyermekeinek nyújtott, legalább is 1899-ig amikor is egy természeti csapás következtében anyagilag tönkrement és a család elszegényedett.
Mihály a kitûnõ Trefort utcai Minta Gimnáziumba járt, ahol 1909-ben érettségizett.6 Olyan pályát kellett választania, ami a család számára biztos anyagi támaszt ígért. Beiratkozott a budapesti egyetem orvoskarára. Már egyetemi tanulmányai elején bekapcsolódott a kutatómunkába Tangl Ferenc, a neves fiziológia professzor irányításával. 1910-tõl jelentek meg elsõ publikációi, amelyek az agyvíz és a vérsavó kémiai összetételének vizsgálatával foglalkoztak. Az orvosi tanulmányait 1913-ban fejezte be és 1914-ben orvos-doktorrá avatták.
Kémiai ismereteinek bõvítése érdekében még orvosegyetemi éveinek befejezése elõtt kémiai tanulmányokat kezdett Karlsruheban, ahová 1912 és 1913-14-ben, Pfeifer Ignác mûegyetemi vegyészprofesszor segítségével sikerült kiutaznia. Egyébként ugyancsak Pfeifer Ignác közbenjárására alkalmazták késõbb Polányi Mihályt tanácsadóként a budapesti Egyesült Izzólámpa Gyárban, amellyel hosszú és eredményes munkakapcsolatot tartott fenn.
Polányi Mihály sokoldalúságát és új iránti fogékonyságát bizonyítja, hogy orvosi és kémiai tanulmányai mellett élénk érdeklõdéssel figyelte az akkoriban kifejlõdõ termodinamika legújabb eredményeit. Sõt nemcsak figyelemmel kísérte, hanem fiatal kora ellenére alkotó módon elõ is segítette ennek a tudományágnak a kibontakozását. 1912 és 1914 között végzett munkássága a kvantumelmélet termodinamikai következményeinek feltárásával, illetve a termodinamika második fõtételének az adszorpcióra történõ alkalmazásával és a harmadik fõtétel megalapozásával foglalkoztak. Ennek a munkának a gyümölcse hat tudományos dolgozat.7-12 Érdekességként említhetõ, hogy 1913-ban a harmadik fõtétellel kapcsolatos gondolatait és megfontolásait elküldte Bredig professzornak, kedvelt karlsruhei tanárának, aki a kéziratot eljutatta Einsteinnek. Einstein válasza az volt: "Nagyon tetszik nekem Polányi úr cikke". Ezzel személyes érintkezés jött létre Polányi és Einstein között, ami az I. világháború alatt és azt követõen is tartott. Levelezésük, ami fõleg a harmadik fõtétellel kapcsolatos kérdésekkel foglalkozott, szívélyes és baráti hangvételû volt.
Közben folyt az I. világháború. Polányi Mihály hazajött Magyarországra és tiszti rangban, katonaorvosként szolgált a hadseregben. A háborút követõen, a Károlyi-kormány idején az egészségügyi minisztérium államtitkára volt, és ebben a minõségében tervet dolgozott ki a magyar egészségügyi ellátási rendszer megreformálására. A Tanácsköztársaság alatt a Budapesti Egyetem III. sz. Fizikai Intézetében dolgozott Hevesy György munkatársaként.
A vesztes háború utáni Magyarország politikai, társadalmi és kulturális viszonyai nem ígértek túl jó perspektívát a fiatal, tehetséges és törekvõ, zsidó származású Polányi Mihály számára. Ezért 1919-ben végleg elhagyta az országot, visszatért Karlsruhéba. Rövid karlsruhei tartózkodása jelentõsnek bizonyult a késõbbiekben mind családi viszonylatban, mind pedig további tudományos pályáját illetõen. Egyrészt ekkor ismerkedett meg Kemény Magdával, aki szintén kémikus volt, és akit késõbb feleségül vett. Másrészt ekkor terelõdött érdeklõdése és figyelme a reakciókinetika, a kémiai reakciók sebességének tanulmányozása felé.
Az adszorpció új elméletének kifejlesztése Polányi Mihály korai munkásságának legfontosabb mérföldköve. Ebben a témakörben írt két közleménye13,14 szolgált doktori értekezésének alapjául, amellyel 1917-ben a Budapesti Mûszaki Egyetemen elnyerte az egyetemi doktori (Ph.D.) fokozatot. Polányi az adszorpció jelenségét teljesen újszerû módon közelítette meg. Feltételezte, hogy az adszorbeáló felület és a gázfázisú atomok, illetve molekulák között ható erõk következtében az adszorpció több rétegben következik be. Az adszorpciós izoterma és hõmérséklet-függésének számítása céljából definiált egy e adszorpciós potenciált, mint annak a j térfogatnak a függvényét, amelyben az e adszorpciós potenciál hat:
e = f (j )
Polányi adszorpciós elmélete ellenvéleményt váltott ki és elutasítására talált kortársai részérõl. Ugyanis a feltételezett nagy hatótávolságú vonzás az adszorbens és a gázmolekulák között érthetetlennek tûnt, mivel akkoriban csak kétféle erõt ismertek, mégpedig az elektrosztatikus és a vegyértékerõket. Ezek pedig nem eredményezhettek többrétegû adszorpciót. Amikor Polányi 1921-ben Berlinben elõadta elméletét, Nernst és Einstein ellenvéleményüket arra hivatkozva fogalmazták meg, hogy az akkor általánosan elfogadott Bohr-féle atomelmélet alapján nem értelmezhetõk a Polányi által feltételezett hosszú hatótávolságú erõk, így az elmélet nyilvánvalóan hibás. Évekkel késõbb Polányi azt írta, hogy ez a szeminárium tudományos pályájának majdnem a végét jelentette. Mindezek ellenére több közleményt jelentetett meg, amelyekben kísérleti bizonyítékokat közölt és további érveket sorakoztatott fel az elmélet alátámasztására. Lényegében azonban a húszas évek végéig, a kvantummechanika kifejlõdéséig kellett várnia, amíg Fritz London segítségével kétségbevonhatatlanul igazolni tudta adszorpciós elméletét a kvantummechanikai alapokon nyugvó diszperziós erõk segítségével.15
 |
| Polányi Mihály, a Kaiser
Wilhelm-Institut für physi- kalische Chemie und Electrochemie osztály- vezetõje |
Az intézetben eltöltött két év alatt Polányi és munkatársai több más érdekes kérdéssel is foglalkoztak, mint pl. a fémkristályok növesztésével, fémek és más kristályos anyagok fizikai tulajdonságainak megváltozásával külsõ erõ alkalmazásának hatására. Jelentõs felismerésekre jutottak a kristályok nyírási, illetve szakítási erõvel szemben mutatott ellenállásával kapcsolatban.
1923-ban fontos változás következett be Polányi Mihály tudományos pályáján. A Nobel-díjas Fritz Haber megbízta az általa vezetett Kaiser Wilhelm Institut für physikalische Chemie und Elektrochemie egyik osztálya munkájának irányításával és egyidejûleg kinevezték a berlini Technische Hochschule tanárává. Megnõsült, feleségül vette Kemény Magdát. Munkahelyén is igen kedvezõ körülmények közé került, tehetséges munkatársak, kitûnõ barátok vették körül, többek között Wigner Jenõ is. A kutatásait nagy kedvvel és lendülettel indította meg a reakciókinetika területén, amely már hosszú évek óta érdekelte és foglalkoztatta. (Megjegyzem, hogy 1920-ban már megjelentetett négy közleményt ebben a témakörben.) Az Insitut für physikalische Chemie und Elektrochemie-ben megkezdett reakciókinetikai kutatásai, amelyek késõbb Manchesterben folytatódtak, hozták meg Polányi Mihály legjelentõsebb tudományos eredményeit. Ezekben a kutatásokban mutatkozott meg leginkább páratlan kreativitása. Kísérleti munkáit szellemes technikai megoldások, elméleti vizsgálatait az igényesség és az új utak keresése jellemezte. Mindezek eredményeként kutatásaival jelentõsen kortársai elõtt járt.

Csoportkép a Fritz Haber által vezetett Kaiser Wilhelm-Institut für physikalische Chemie und Electrochemie tagjairól. Polányi Mihály Fritz Haber bal oldalán foglal helyet.
Kísérleti munkáinak jelentõs részében Polányi és munkatársai atomok és molekulák között lejátszódó elemi reakciók sebességét tanulmányozták. Az akkori idõk kísérleti technikájának fejlettsége nem tette lehetõvé gyors reakciók sebességének meghatározását. Ezért Polányi és munkatársai kifejlesztették a gyors reakciók vizsgálatára is alkalmas ún. "nagy ritkítású atomi láng" módszert.18-20 Megjegyzendõ, hogy a módszer kifejlesztéséhez és alkalmazásához két magyar származású kutató, S. von Bogdandy és Schay Géza, is jelentõs mértékben hozzájárult. Ez a kísérleti technika igen eredményesnek bizonyult atomok és molekulák között lejátszódó reakciók sebességének, sebességi állandójának meghatározásában. Ennél is figyelemre méltóbb azonban az, hogy a nagy ritkítású atomi láng módszer a D. R. Herschbach és Y. T. Lee által jóval késõbb kifejlesztett keresztezett molekulasugár módszer elõfutárának tekinthetõ, amelyért a felfedezõk 1986-ban elnyerték a kémiai Nobel-díjat.
Kísérleti kutatásai mellett Polányi nagyon fontos feladatnak tartotta a reakciósebességi elméletek továbbfejlesztését. Ismeretes, hogy már az 1920-as években foglalkoztatta az az ellentmondás, amely az akkor rendelkezésre álló kinetikai elméletek és a termodinamika között észlelhetõ volt. Karlsruhei éveinek elsõ jelentõs elméleti eredménye a disszociációs és asszociációs reakciók sebességi elméletének kidolgozása, amit Wigner Jenõvel együtt valósított meg.21 (Itt jegyzem meg, hogy ezekben az években a késõbbi Nobel-díjas Wigner Jenõ Polányi Mihály diákja volt.) Az igazán nagy eredményt azonban a potenciálisenergia-felület és az átmeneti állapot fogalmak bevezetése és az átmenetiállapot-elmélet kifejlesztése jelentette.
Az átmenetiállapot-elmélet kifejlesztésének lehetõsége akkor tárult fel, amikor Fritz London 1928-ban kifejtette a kémiai kötés kvantummechanikai elméletét.22 A London-féle elméletre támaszkodva Polányi Mihály és Henry Eyring, aki ez idõ tájt Berlinben dolgozott Polányi munkatársaként, megszerkesztették egy reagáló rendszer elsõ potenciálfelületét.23,24 Egy ilyen potenciálfelületet mutatok be vázlatosan az 1. ábrán egy A + BC > AB + C általános alakban felírt kémiai reakció jellemzésére. Ez a szintvonalas ábrázolás a potenciális energiát mutatja be a képzõdõ AB, valamint a felhasadó BC kötéstávolságok függvényében (az ABC részecskék által bezárt szöget állandó értéken, 180o-nál rögzítve). A görbék egyenlõ energiájú pontokat kötnek össze és a növekvõ számok növekvõ energiát jelképeznek. Tulajdonképpen ez a felület torzított nyeregfelület, amely két völgybõl áll: egy reaktáns völgybõl (nagy rAB atomtávolságoknál) és egy termékvölgybõl (nagy rBC atomtávolságoknál), a két völgy érintkezési pontja (a völgyek mélyén vezetõ út legmagasabb pontja) az ún. "átmeneti állapot".
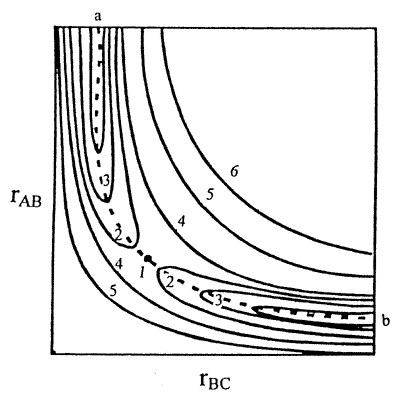
A potenciálisenergia-felület számításának kérdése azért foglalkoztatta Polányit, mert egy olyan eszközt látott benne, amely lehetõvé teszi az elemi kémiai reakció lefolyásának atomi szintû leírását. A kémiai reakció végbemenetele úgy szemléltethetõ, mint egy golyó pályája a potenciálfelületen. A golyót meglökve elindítjuk a reaktáns völgybõl, az a-val jelölt kiindulási állapotból. Amennyiben a feltételek megfelelõek, a golyó pályája az 1-gyel jelölt átmeneti állapoton keresztül átvezet a termékvölgybe, a b-vel jelölt végállapotba. Tehát végbement a kémiai reakció.
Ilyen gondolatok foglalkoztatták Polányi Mihályt és munkatársait a berlini intézetben. Az átmenetiállapot-elmélet alapgondolatát Marcelin25 korábbi javaslatát kifejtve az osztály két munkatársa H. Pelzer és Wigner Jenõ26 alkalmazta elõször 1932-ben, amikor is az Eyring és Polányi által számított potenciálisenergia-felület felhasználásával sikerült kiszámítaniuk több elemi reakció átmeneti állapotának fizikai sajátságait.
 |
| Polányi Mihály, a manchesteri
egyetem tanára |
Mindezen szerteágazó munkái mellett is egyik legkedveltebb kutatási területe az elméleti reakciókinetika mûvelése, különösen az átmenetiállapot-elmélet kifejlesztése maradt. Legközelebbi munkatársával, legjobb barátjával Meredith Evansszel együttmûködve, a Pelzer és Wigner féle megközelítést alkalmazva, 1935-ben sikerült kvantitatív formában megfogalmazniuk az átmenetiállapot-elméletet.27-30 Egyidejûleg és velük párhuzamosan munkálta ki az Egyesült Államokban Henry Eyring31, részben Wynne-Jonesszal együttmûködve32, hasonló reakciósebességi elméletét, amelyet "aktivált komplex elméletnek" nevezett. Ezzel elindult hosszú és példátlan diadalútjára az átmenetiállapot-elmélet, amely még ma, 65 év után is meghatározó jelentõségû az adott tudományterületen.
Polányi Mihály érdeklõdésének középpontjában állott a reakciókinetika és a termodinamika, és pályájának kezdetétõl foglalkoztatta a reakciókinetika és termodinamika lehetséges kapcsolata. Ez utóbbi területen szintén Evansszal együttmûködve érte el legjelentõsebb eredményét. Megállapították ugyanis, hogy egy homológ reakciósorban, mint például a Na-atom és különféle bromidok (alkil-bromidok, HBr, és Br2) között lejátszódó reakciókban, ahol NaBr képzõdik, összefüggés állapítható meg a reakciók aktiválási energiája (Ea) és a reakció exotermicitása (DH) között.33,34 Ezt az összefüggést a következõ alakban írták fel:
Ea = aDH + c
Az összefüggés érvényességét a 2. ábrán mutatom be a Na-atom és alkil-halogenidek reakcióira. Késõbbi kutatások az összefüggést számos homológ sorra érvényesnek találták és felhasználták, például reakcióhõk és kötésdisszociációs energiák becslésére. Ez az egyszerû összefüggés, amely EvansPolányi összefüggés néven ismert, hosszú idõn keresztül a kémiai kinetika legnépszerûbb egyenletei közé tartozott.
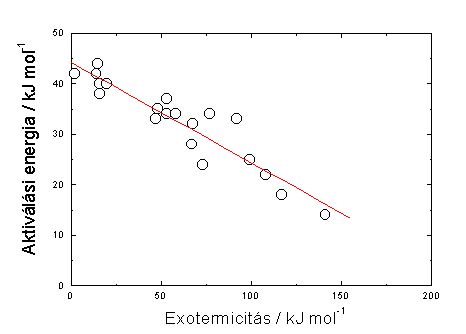
2. ábra. Az aktiválási energia ábrázolása a reakcióhõvel szemben a Na-atom és alkil-halogenidek homológ reakciósorában (EvansPolányi összefüggés)
Nem lenne teljes ismertetésem Polányi Mihályról a fizikokémikusról és reakciókinetikusról, ha nem emlékeznék meg a reakciómechanizmusokkal kapcsolatosan kifejtett jelentõs tevékenységérõl. Ez a munka már az 1920-as évek elején megkezdõdött a H2 és Br2 közötti reakció mechanizmusának kutatásával. Polányi Mihály, Herzfelddel és Christiansennel együtt, jelentõs szerepet játszott a láncreakciók elméletének kimunkálásában. Egyik utolsó kémiai tárgyú munkája is ezzel a témakörrel foglakozott, amely 1949-ben "Mechanism of chemical reactions" címmel jelent meg.35
Ezt követõen Polányi Mihály nem írt több kémiai tárgyú munkát, 1946-ban feladta kémiai katedráját és a manchesteri egyetem Social Studies tanszéken Polányi Mihály, a filozófus kezdte meg ugyancsak jelentõs pályáját. Nyitott kérdés az, hogy mi késztette Polányi Mihályt erre a váltásra. Nyilván szerepet játszott ebben régrõl fennálló érdeklõdése a filozófia és közgazdaságtan iránt.
A manchesteri egyetemen filozófusként dolgozott 1958-ig, nyugdíjazásáig. 1951 és 1958 között írta meg filozófiai fõmûvét36, amely "Personal Knowledge" címen jelent meg. 1959 és 1961 között a híres oxfordi Merton College-ban kutatói állást (senior research fellow) töltött be. 1976. február 22-én hunyt el az angliai Northamptonban.
Ismertetésemet itt azzal szeretném zárni, hogy Polányi Mihályt, a kimagasló tudóst, a kreatív fizikokémikust, feltétlenül a huszadik század elsõ felének azon kivételes tehetségû magyar természettudósokból álló csoport tagjaként kell számon tartanunk, amelyhez többek között Hevesy György, Szent-Györgyi Albert, Neumann János, Teller Ede és Wigner Jenõ is tartozott.
E. P. Wigner and R. A. Hodgkin, "Michael Polanyi, 1891-1976", Biographical Memoirs of Fellows of the Royal Society, 23, 413 (1977).
W. T. Scott, "Michael Polanyi's Creativity in Chemistry", in P. Ignotus et al., "The Logic of Personal Knowledge": essays presented to Michael Polanyi on his seventieth birthday, Routledge and Kegan, London, 1961, p. 279.
Palló G., "A kémikus és filozófus Polányi Mihály", Magyar Tudomány, 1991/4, 489.
J. C. Polányi, "An Index to Michael Polanyi's Contribution to Science", in P. Ignotus et al., "The Logic of Personal Knowledge": essays presented to Michael Polanyi on his seventieth birthday, Routledge and Kegan, London, 1961, p. 15.
P. Ignotus, "The Hungary of Michael Polanyi", in P. Ignotus et al., "The Logic of Personal Knowledge: essays presented to Michael Polanyi on his seventieth birthday", Routledge and Kegan, London, 1961, p. 12.
G. Palló, "Michel Polanyi's Early Years in Science", Bull. Hist. Chem., 21, 39 (1998).
J. Baron and M. Polanyi, "On the Application of the Second Law of Thermodynamics to Processes in the Animal Organism", Biochem. Z., 53, 1 (1913).
M. Polanyi, "A new Thermodynamic Consequence of the Quantum Hypothesis", Verh. Deut. phys. Ges., 15, 156 (1913).
M. Polanyi, "New Thermodynamic Consequences of the Quantum Hypothesis", Z. phys. Chem., 83, 339 (1913).
M. Polanyi, "Adsorption and Capillarity from the Standpoint of the Second Law of Thermodynamics", Z. phys. Chem., 88, 622 (1914).
M. Polanyi, "On the Adsorption from the Standpoint of the Third Law of Thermodynamics", Verh. deut. phys. Ges., 16, 1012 (1914).
M. Polanyi, "On the Derivation of Nernst's Theorem", Verh. deut. phys. Ges., 17, 350 (1915).
M. Polanyi, "Adsorption of Gases by a Solid Non-Volatile Adsorbent", Verh. deut. phys. Ges., 18, 55 (1916).
M. Polanyi, "On the Theory of Adsorption", Magyar Kémiai Folyóirat, 23, 3 (1917).
F. London and M. Polanyi, "The Theoretical Interpretation of Adsorption Forces", Naturwissenschaften, 18, 1099 (1930).
M. Polanyi, R. O. Herzog and W. Jancke, "On the Sturcture of the Celluose and Silk Fibre", Z. Physik, 20, 413 (1923).
M. Polanyi, E. Schiebold and K. Weissenberg, "On the Development of the Rotating Crystal Method", Z. Physik, 23, 337 (1924).
H. Beutler and M. Polanyi, "On Highly Dilute Flames, I. Flame in Simple Tube", Z. phys. Chem, B1, 3 (1928).
S. von Bogdandy and M. Polanyi, "On Highly Dilute Flames, II. Nozzle Flames. Increase of Light Emission with Increasing Partial Pressure of Sodium Vapour", Z. phys. Chem, B1, 21 (1928).
M. Polanyi and G. Schay, "On Highly Dilute Flames, III. Sodium-Chlorine Flame. Evidence for and Analysis of the Reaction and Luminescence Mechanism. Both Reaction Types. Survey of the Whole Work". Z. phys. Chem, B1, 30 (1928).
M. Polanyi and E. Wigner, "Formation and Decomposition of Molecules", Z. Physik, 33, 429 (1925).
F. London, "Probleme der modernen Physik", Sommerfeld Festschrift, ed. S. Herzel, Leipzig, 1928, p. 104.
M. Polanyi and H. Eyring, "On the Calculation of Energy of Activation", Naturwissenschaften, 18, 914 (1930).
H. Eyring and M. Polanyi, "On Simple Gas Reactions", Z. phys. Chem., B12, 279 (1931).
A. Marcelin, Ann. Phys. (Paris), 3, 158 (1915).
H. Pelzer and E. Wigner, Z. phys. Chem., B15, 445 (1932).
M. G. Evans and M. Polanyi, "Some Applications of the Transition State Method to the Calculation of Reaction Velocities, Especially in Solution., Trans. Faraday Soc., 31, 875 (1935).
M. G. Evans and M. Polanyi, "On the Introduction of Thermodynamical Variables into Reaction Kinetics", Trans. Faraday Soc., 33, 448 (1937).
M. Polanyi, "The Transition State in Chemical Reactions", J. Chem. Soc., 629 (1937).
M. Polanyi, " The Transition State in Chemical Kinetics", Nature London, 139, 575 (1937).
H. Eyring, "The Activated Complex in Chemical Reactions", J. Chem. Phys. 3, 107 (1935).
W. F. K. Wynne-Jones and H. Eyring, "The Absolute Rate of Reactions in Condensed Phases", J. Chem. Phys, 3, 492 (1935).
M. G. Evans and M. Polanyi, "Further Consideration on the Thermodynamics of Chemical Equilibria and Reaction Rates", Trans. Faraday Soc., 32, 1333 (1936).
M. G. Evans and M. Polanyi, "Inertia and Driving Force of Chemical Reactions", Trans. Faraday Soc., 34, 1138 (1938).
M. Polanyi, "Mechanism of Chemical Reactions", Endeavour, 8, 3 (1949).
M. Polanyi, "Personal Knowledge", London: Routledge and Kegan Paul, 1958; Chicago: University Press 1958.